|
|
Категория:
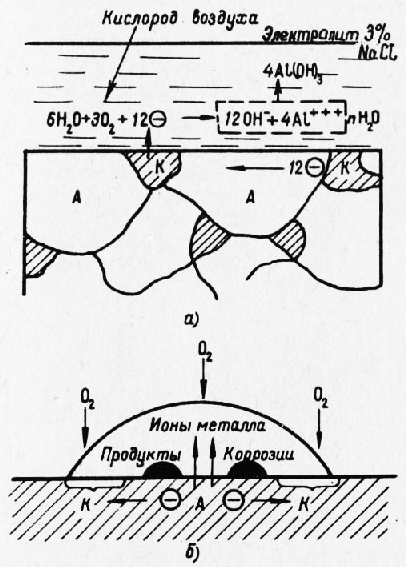
Цветные металлы В качестве примеров электрохимической коррозии можно рассмотреть работу гальванических микропар, коррозию под каплей влаги и разрушение подземных конструкций. Гальванические микропары. В основе развития процессов электрохимической коррозии сплава при наличии в нем двух или нескольких разнородных фаз лежит деятельность большого числа микрогальванических элементов или микропар. Процессы, протекающие на микроэлектродах, аналогичны ранее рассмотренным процессам работы гальванической пары из двух различных металлов. Так, например, в отожженном алюминиево-медном сплаве, имеющем двухфазную структуру и находящемся в соприкосновении с 3%-м раствором NaCl (рис. 1,а), коррозионному разрушению подвергается твердый раствор, имеющий потенциал—0,60 в и являющийся анодом по отношению к включениям СиА12, потенциал которых — 0,37 в. Химическое соединение, являющееся катодом, не разрушается. Процесс протекает с кислородной деполяризацией на катоде. При работе микропары с анода в раствор переходят ионы алюминия. На катоде образуются гидроксильные ионы ОН. Продукт коррозии представляет собой гидрат окиси алюминия А1(ОН)3.
Рис. 1. Схема электрохимической коррозии:
а — двухфазного сплава; б — чистого металла под каплей влаги
Коррозия под каплей влаги. При эксплуатации изделий на поверхности металла возможно оседание мелких водяных капель. При растворении в этих каплях атмосферных газов образуется электролит. Особенно вредными являются: для стали — сернистый газ, сероводород и хлористый водород; для алюминиевых и магниевых сплавов — хлористый водород; для медных сплавов — аммиак. Коррозия под каплей влаги (рис. 1,б) развивается в результате неоднородности пассивирования отдельных участков поверхности металла под каплей по причине неодинакового доступа кислорода воздуха. Вследствие большого притока кислорода к периферийным участкам поверхности под каплей последние находятся в более пассивном состоянии, чем центральные участки. Железо, например, в активном состоянии имеет потенциал от —0,4 до —0,5 в, а в пассивном +1,0 в и более. Поэтому разрушению подвергаются центральные участки, потенциал которых имеет более отрицательное значение. Разрушение подземных конструкций. Увлажненная земля обычно является проводником тока и, находясь в контакте с металлическими конструкциями, способствует развитию в них электрохимической коррозии. Большое влияние на коррозию подземных сооружений оказывают «блуждающие токи». Вредное влияние имеет только постоянный ток, ответвляющийся, например, от рельсовых путей электрических железных дорог, заземлений установок, питаемых постоянным током, и т. д. При этом участок вхождения тока является катодной зоной и коррозионному разрушению не подвергается, а участок выхода блуждающих токов из металла в почву представляет собой анодную зону, подверженную коррозионному разрушению в виде глубоких местных раковин. Реклама:Читать далее:Выбор химического состава и обработкиСтатьи по теме:Главная → Справочник → Статьи → Блог → Форум |
|
|
|
|
Контакты: Сергей Королёв © 2007-2009 Pereosnastka.ru - информационный сайт о металло- и деревообработке. |
© Все права защищены.
Копирование материалов невозможно. |
|