|
|
Категория:
Литейное производство Далее: Процесс легирования Металлы отличаются от других твердых тел наличием свободных электронов. Эти электроны не связаны с каким-то определенным атомом и движутся по всему металлу. Свободные электроны определяют такие свойства металлов, как пластичность, электропроводимость и др. Специфика твердого металлического состояния, в основном, сохраняется и после расплавления. Особый характер так называемой металлической связи приводит к возможности образования различных смешанных кристаллов (сплавов). Процесс плавления металлов и сплавов является достаточно сложным из-за «накладывающихся» друг на друга различных физико-химических явлений, однако, его сущность легче представить, чем процесс кристаллизации. Это объясняется тем, что плавление не требует образования зародышей, и процесс перехода из твердого состояния в жидкое начинается сразу же, как только металл или сплав будет нагрет до температуры начала плавления. Некоторый перегрев выше температуры плавления необходим для того, чтобы расплавление кристалла началось внутри него. Плавление — относительно простой процесс еще и потому, что жидкий сплав имеет строение, малозависящее от условий его образования. В твердой плавящейся фазе практически не происходит перераспределения химических веществ. Известно, что кристаллическим телам свойственна строгая периодичность в расположении частиц. В то же время силы, удерживающие атомы в узлах кристаллической решетки, очень малы. Достаточно тепловой энергии самих атомов, чтобы они отклонялись от равновесного положения на заметные расстояния. Установлено, что при обычной температуре величина теплового колебания может составлять 5-10% межатомного расстояния. Наиболее существенными способами поглощения тепловой энергии твердыми металлическими телами являются способы увеличения: При нагревании металлов и сплавов от обычной температуры ДО температуры плавления происходит непрерывное поглощение энергии, которая расходуется на увеличение интенсивности указанных колебании и движений. До какого-то момента времени каждый атом находится на своем обычном месте и окружен соответствующим числом ближайших атомов, расположенных на расстояниях, примерно соответствующих совершенной структуре. Но наступает момент, когда эти расстояния нарушаются или у атома изменяется число соседних атомов. Этот период предплавления характеризуется значительным ростом дефектов структуры различного вида.
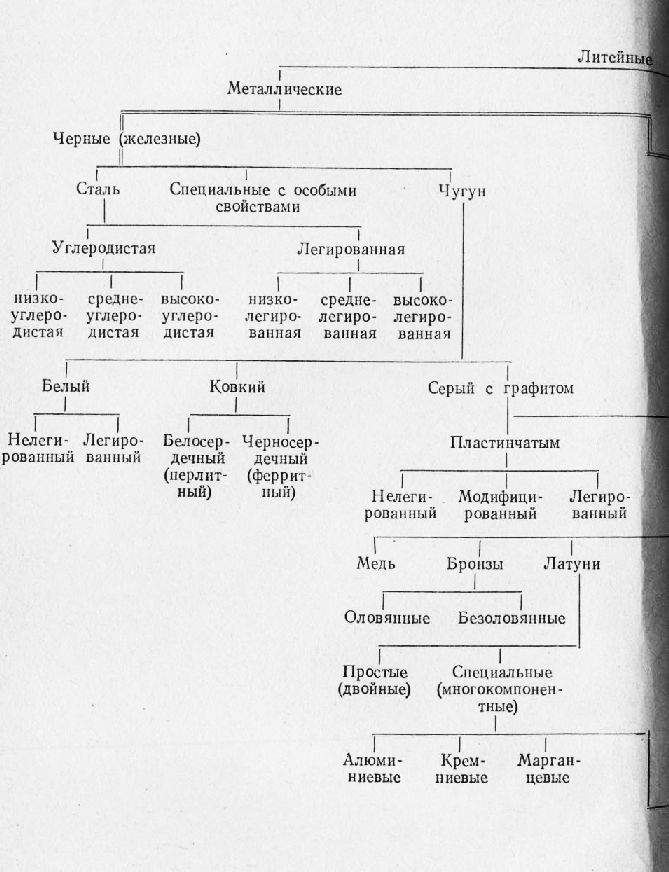
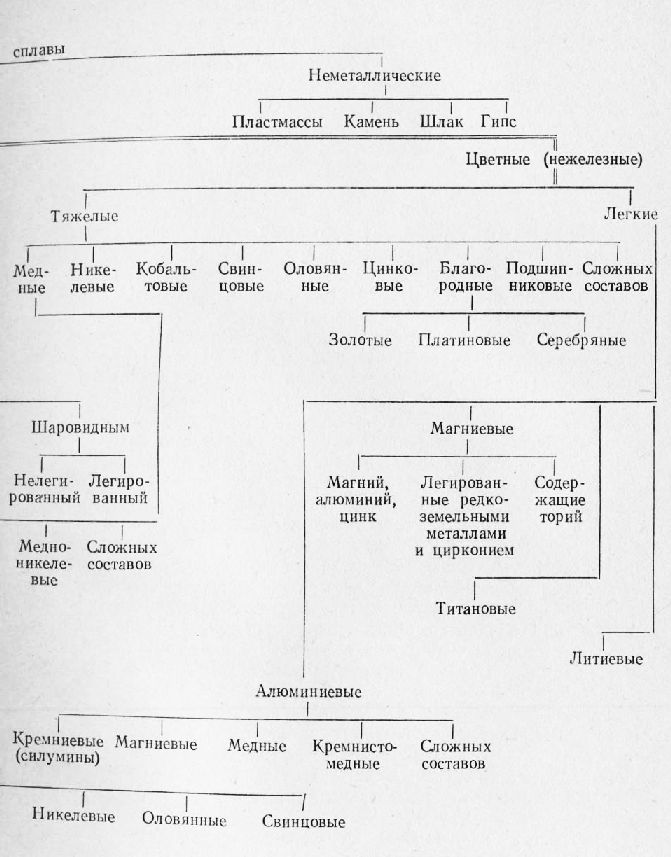
Схема 1. Классификация литейных сплавов
Из приведенного следует, что количество вакансий зависит главным образом от температуры. Например, у алюминия одна вакансия приходится на 1012 атомов при комнатной температуре, а при температуре плавления — только на 103 атомов. Для алюминия Еа = 0,75 эв. Следует отметить, что наличие одной вакансии на 1000 атомов типично для твердых металлов вблизи температуры плавления. Особенность предплавления — значительная интенсификация диффузионных процессов — связана с тем, что атомы получают возможность перемещаться на большие расстояния вследствие увеличения количества вакансий и их передвижения. При плавлении нарушаются термодинамическая устойчивость кристаллических решеток и характерный для твердого состояния порядок расположения атомов (молекул или ионов). В результате твердые кристаллические тела теряют постоянство формы, происходит скачкообразное изменение (увеличение) внутренней энергии, объема, энтропии и некоторых других физических свойств металлов и сплавов. Сплавы, в отличие от однокомпонентных веществ, плавятся в некотором интервале температур, зависящем от их состава и давления. Тепло, образующееся в плавильных агрегатах в результате горения топлива или иного процесса, передается твердой металлической шихте и, в первую очередь, расходуется на тепловое расширение, являющееся следствием увеличения колебательного движения атомов относительно их обычного равновесного положения. С повышением температуры колебательные движения увеличиваются и твердое тело, проходя через область неустойчивых состояний, превращается в жидкое. Чтобы этот процесс мог завершиться полностью, в рабочее пространство печи должно поступать количество теплоты, необходимое для обеспечения отрыва атомов от их обычного равновесного положения и для компенсации различных потерь теплоты сопутствующих плавлению процессов. Следовательно, плавление можно рассматривать как переход из состояния, при котором атомы в кристаллической решетке рас-положены правильно, в состояние, при котором решетка уничтожается. Отметим, что переход в жидкое состояние не всегда приводит к полному уничтожению кристаллической структуры. Еще в 1921 г. А. А. Лебедев показал, что и в жидкостях можно встретить некоторую упорядоченность расположения молекул, выражающуюся в том, что в отдельных ультрамикроскопических участках объема молекулы образуют ничтожно малые по размерам кристаллиты. Такие образования в жидкостях обнаруживаются при температурах, близких к температуре плавления. Полное уничтожение остатков кристаллического строения может быть достигнуто только при дальнейшем повышении температуры и длительной выдержке расплава. Особенностью многих процессов плавки в литейном производстве является необходимость достижения температур превращения твердой шихты в состояние, при котором в максимально возможной степени были бы уничтожены остатки структуры твердого состояния. Это обеспечивает получение, например, требуемых механических свойств у многих сплавов, в частности у чугуна. При плавлении объем металлов увеличивается на 3-4%, что необходимо учитывать при изучении кристаллизации отливок в литейных формах. Следует подчеркнуть, что для качества будущей отливки небезразлично с какой интенсивностью и в какой среде производится плавление, а также какая степень перегрева выше температуры плавления была при этом достигнута. Перечисленные факторы могут в последующем оказать решающее влияние на процесс кристаллизации отливки и конечные ее свойства. Например, большое влияние на кристаллизацию оказывают имеющиеся в расплаве частицы (подложки), образующие поверхность раздела. Они могут служить источником гетерогенного зарождения кристаллов. На этой поверхности, если она смачивается жидким металлом, могут образоваться зародыши и их образование потребует меньшей затраты энергии. Большое значение имеет и краевой угол смачивания между подложкой и находящимся на ней зародышем твердой фазы. Если краевой угол смачивания 0 мал, то поверхностная энергия границы раздела между твердой фазой и подложкой также мала. В этом случае из атомов жидкого металла легко образуются зародыши твердой фазы на поверхности подложки. Когда 0 = 180°, подложка существенно не влияет на процессы зарождения потому, что межфазная энергия на границе твердой фазы и подложки оказывается достаточно большой. Если краевой угол смачивания мал, то зарождение происходит Ри незначительном переохлаждении, если же краевой угол велик, 0 необходимо большое переохлаждение. Практически все литейные сплавы в жидком состоянии содержат определенное количество мельчайших нерастворимых примесей, которые могут оказать влияние на условия кристаллизации. Именно поэтому сплавы (в жидком и твердом состояниях) следует отнести к коллоидным системам. Особенностью коллоидных систем такого рода является их по-лидисперсность. Характер образующейся системы и ее способность к тем или иным взаимодействиям непосредственно связаны с условиями плавления и перегрева металла или сплава. Многие литейные сплавы, особенно цветные, содержат легкоиспаряющиеся компоненты. В литейном производстве поэтому широко используют плавку в вакууме. При любой температуре выше абсолютного нуля все вещества, в основном жидкие, испаряются. Молекулярно-кинетическая теория дает объяснение этому явлению. На поверхности жидкости или твердого тела энергия отдельных молекул значительно превышает среднюю для данной температуры. Эта энергия может быть достаточной для отрыва молекул и рассеивания их в окружающем пространстве. Скорость испарения вещества определяется давлением его пара, зависящим от температуры, и внешним давлением других газов (например, воздуха) над испаряющимся веществом. Давление пара испаряющегося вещества зависит от его природы, температуры и кривизны поверхности и почти не зависит от давления других газов над испаряющимся веществом. Однако скорость диффузии пара, влияющая на общую скорость испарения, уменьшается с увеличением давления постороннего газа в системе. Это обстоятельство учитывают и используют в реальных плавильных процессах для уменьшения потерь легкоиспаряющихся компонентов сплава. Скорость испарения можно значительно снизить, если свободную поверхность испаряющейся жидкости покрыть поверхностно-активным слоем достаточно большой толщины. Слой шлака на жидком металле затрудняет испарение и является желательным при обычной плавке. Ппи таком равновесии число молекул, проникающих за единицу племени через единицу поверхности раздела из жидкости в пар, панно числу молекул, переходящих из пара в жидкость. Упругость насыщения пара каждого вещества зависит только от температуры и повышается с ее увеличением. Удалению паров с поверхности испарения способствует постоянная «вентиляция» этой поверхности вызываемая различными причинами (движением пламени, продуктов горения, подсевом воздуха и т. п.). Чем больше турбулентность движения газового потока над испаряющимся телом, тем больше удаляется пара и скорее протекает процесс испарения. Если давление насыщенного пара становится равным внешнему давлению или несколько его превышает, испарение идет не только с поверхности жидкости, но и внутри нее. При этом образуются пузыри пара, быстро растущие и поднимающиеся на поверхность. Испарение переходит в кипение. Изучение физико-химических закономерностей испарения имеет большое практическое значение для плавки в условиях вакуума. Реклама:Читать далее:Процесс легированияСтатьи по теме:Главная → Справочник → Статьи → Блог → Форум |
|
|
|
|
Контакты: Сергей Королёв © 2007-2009 Pereosnastka.ru - информационный сайт о металло- и деревообработке. |
© Все права защищены.
Копирование материалов невозможно. |
|